科学技術振興機構(JST)は7月23日、東海大学の協力を得て、急性白血病細胞の分化異常を修復するRNAを発見し、白血病細胞を正常化させる可能性を示したと発表した。
成果は、東海大学 医学部の幸谷愛 准教授、同・奥山一生研究員らの研究チームによるもの。研究はJST課題達成型基礎研究の一環として行われ、詳細な内容は米国東部時間7月22日付けで米科学雑誌「米科学アカデミー紀要(PNAS)」に掲載された。
白血病は、未熟な白血球が異常増殖してしまう「血液のがん」で、国内でも年間約8700人が罹患している(地域がん登録全国推計によるがん罹患データ1997年~2002年)。発症の仕方によって「急性白血病」と「慢性白血病」の2種類があり、急性白血病の原因として考えられているのが、遺伝子の異常だ。細胞増殖に関わるClass1遺伝子群、細胞分化に関わるClass2遺伝子群の両方の制御ができなくなることで発症するというものである。Class1遺伝子の異常では細胞増殖が進み、Class2遺伝子の異常では分化が障害されることが多い。
一般に、細胞の分化には「転写因子」と呼ばれるタンパク質が重要な働きをすると考えられており、血液細胞の分化においても、さまざまな転写因子が同定されている。急性白血病では、転写因子の異常による分化障害が発症の引き金となるため、その異常を修復し、正常化することにより白血病細胞を脱がん化させる可能性があるという。
一方、2003年に完了宣言がなされた最初の「ヒトゲノムプロジェクト」によって、タンパク質に翻訳される遺伝子のみでは、ヒトの多様性を説明することができないことがわかってきた。それを説明するための1つのカギと注目されているもの1つに、「非コードRNA(ncRNA)」がある。非コードRNAは、従来の遺伝子配列とは見なされない、タンパク質に翻訳されないDNA配列から転写されるRNAだ。
種によってタンパク質に翻訳される遺伝子領域の数には、大きな差がないことがゲノムプロジェクトによって明らかになり、これまで「ゲノムのごみ」と考えられてきたDNA配列から転写される非コードRNAの多様性に、ヒトらしさを見出す研究が、現在では世界中で盛んに行われている。非コードRNAの1つであるマイクロRNA(miRNA)は、これまで生物学的に重要な機能を持つことが、多数報告されてきているところだ。
またB細胞は血液細胞の1種で、急性白血病の中にはB細胞の分化障害が原因で発症するものが多く含まれる。そして、「造血前駆細胞」からB細胞へ分化する際に必要と考えられている転写因子がClass2遺伝子の1つである「EBF1」だ。さらに、細胞分化の過程においても、miRNAの関与が報告されているが、これまではあくまで転写因子を補佐する働きにとどまると考えられてきていた。
「MLL-AF4(MLL遺伝子再構成陽性)急性白血病細胞」において、発現が低下していることが知られていたmiRNAの1種が、「miR-126」である。そこで研究チームは、まず白血病細胞にmiR-126を導入し、B細胞のマーカータンパク質の発現を調べることにした。すると導入して8週培養後に、miR-126をB細胞マーカーであるCD20のたんぱく発現やB細胞関連遺伝子の発現が上昇が確認され、つまりその白血病細胞がB細胞に分化することが判明したのである(画像1)。これに対し、骨髄系細胞関連遺伝子の発現は変化しない。
また正常マウスの造血前駆細胞にmiR-126とコントロールを導入し、同一系統マウスに移植した場合、miR-126導入細胞移植マウスにおいてB細胞が増加し、T細胞、骨髄系細胞は減少する。つまり、miR-126の導入によって、正常な造血細胞もB細胞へ分化誘導されたのである(画像2)。
|
|
|
|
画像1。miR-126は白血病細胞をB細胞に分化誘導する。**は統計的に差が有意であることを示している |
画像2。miR-126は正常造血前駆細胞もB細胞に分化誘導する。**は統計的に差が有意であることを示している |
次に、miR-126が白血病細胞の分化を誘導するメカニズムが調べられた。すると、miR-126を導入してB細胞に分化する際に、B細胞の分化に必須とされる転写因子EBF1の発現がまったく変わらないことが判明。これは、miR-126が従来知られていなかった、転写因子EBF1を介さないメカニズムによってB細胞分化を誘導している可能性を示唆しているということである。
そこで、EBF1が欠損している造血細胞にmiR-126を導入し、B細胞分化に重要な細胞外因子(「Kitl」、「Flt3l」、「Il7」)を含む培地で培養した。すると、この転写因子欠損造血前駆細胞は、そのままではまったくB細胞に分化できないが、miR-126によってB細胞関連遺伝子(「Pax5」、「Cd79a」、「Cd79b」、「Rag1」、「Rag2」)や、B細胞マーカーの発現が上昇したのである(画像3)。 この結果から、miR-126は転写因子とは無関係に、造血前駆細胞をB細胞に分化させることがわかった。
また、B細胞などの白血球は、造血幹細胞から、画像4のような段階を経て分化する。それぞれの段階で特定の転写因子(赤字)が働くことによってさまざまな遺伝子が誘導され分化が進行する仕組みだ。
今回の研究では、B細胞が成熟する過程の内、プロB細胞からプレB細胞に分化する段階に必須とされる、転写因子EBF1を欠損した細胞を用いて、転写因子とは独立したmiRNA(miR-126)の細胞分化誘導能が検討された。その結果、miR-126が転写因子Ebf1の欠損を補い得ることが見出されたのである。つまり、転写因子とは無関係に、miRNAによってB細胞分化障害が正常化され、B細胞方向への分化誘導が起こり得ることが示されたというわけだ。
そして、白血病細胞をB細胞へと分化誘導する非コードRNAも同定された。従来の転写因子を中心とした「細胞運命」(1つ1つの細胞がその元となる幹細胞から生み出され、組織や臓器になる(分化する)過程で、"どのような細胞になるのか"が決定されること)の決定についての考え方に、新たに非コードRNAの重要性を加えられる可能性があるという。さらに、白血病においては転写因子の異常による分化障害が発症の引き金となるため、非コードRNAによりその異常を修復し、正常化することは白血病細胞を脱がん化させる可能性があるとしている。
非コードRNAの1種、miRNAはほ乳類では2000年に発見されたばかりの新しい研究分野であり、まだ治療応用で臨床試験が進行しているものはわずかだ。しかし従来の遺伝子と異なり、複数の遺伝子を制御する点がユニークであること、生物製剤であるため、比較的毒性が低いことなど、新しい治療標的として魅力的な分野と考えられるという。
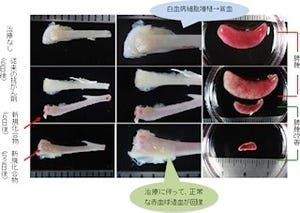
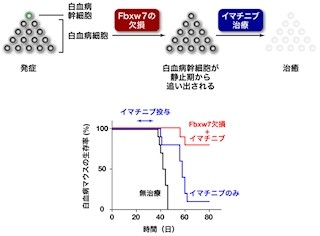
今回の研究では、EBF1の異常による分化障害をmiRNAで回復させることを証明した。よって、miRNAを用いて分化障害を回復させることにより、白血病細胞を治療できる可能性があるとしている(画像5)。