科学技術振興機構(JST)と岡山大学は6月5日、有尾両生類で四肢を再生させることのできる3因子を発見したと共同で発表した。
成果は、岡山大 異分野融合先端研究コアの佐藤伸准教授らの研究チームによるもの。研究はJST課題達成型基礎研究の一環として行われ、詳細な内容は近日中に米国科学誌「Developmental Biology」に掲載される予定だ。
ヒトを含む高等脊椎動物には、説明するまでもなく高次構造である「器官」を再生する能力はなく、1度失われると、iPS細胞技術を用いたとしても至難の業だ。ところが、有尾両生類といわれるメキシコサラマンダ―(通称:ウーパールーパー)は、手足などの器官再生という、高次構造の機能回復をいとも簡単に行える動物として知られている。今回の研究では、これらの動物とヒトとの差異を明らかにしていくことで、ヒトが潜在的に持っている再生能力を引き出すこと大きな目的として行われた。
四肢再生メカニズムに関しては、佐藤准教授らのこれまでの研究により、必要な組織間相互作用までは特定されていた。再生の開始に必要なのは「皮膚の損傷」と「神経の存在」の2つだ。単純な皮膚損傷では、再生動物のウーパールーパーでも、高等脊椎動物と同様に皮膚の修復しか行いない。ところが、皮膚損傷に次いで人為的に神経を配置させると、単純な皮膚修復から四肢再生へ向けた反応が進行し始めるのだ。このことから、神経の存在が再生開始をコントロールしていることは示されたが、具体的にどのような因子が関わっているのかは不明だった。
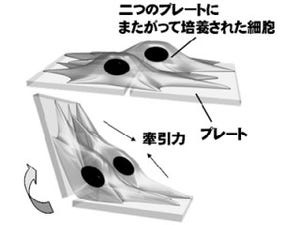
そのメカニズムを解明するため、佐藤准教授らは四肢再生研究で有効な実験システム「過剰肢付加モデル」を使用して研究を進めた。過剰肢付加モデルとは、本来肢(あし)ではない箇所に過剰な肢を追加的に誘導するユニークな実験系だ(画像1)。
この実験系を利用して、次世代DNAシーケンサーで皮膚損傷時と再生反応進行時の遺伝子発現の比較が行われた。これまでの知見から神経からの分泌因子が再生開始を制御していると強く示唆していたため、分泌因子に絞って候補因子の選定を実施し、大きく2つの遺伝子の情報伝達経路「FGF-シグナリング」と「TGF-β-シグナリング」に着目するに至ったのである。
その中でFGF-シグナリングの重要性は、すでに佐藤准教授らの研究成果で示していることから、はじめにTGF-β-シグナリングに関する研究を進め、「GDF5タンパク質」が皮膚損傷から再生開始のサインである「再生芽」様の構造を誘導し得ることが発見された(画像2)。
皮膚損傷後は、通常であれば皮膚の修復が起こるのみだが、GDF5タンパク質を損傷後の皮膚に添加したところ、皮膚修復時には起こらない伸長反応が観察された。しかし、神経を遊走させた場合では、この再生芽が伸長を続けて最終的に四肢を形成するのに対し、GDF5によって誘導した再生芽様構造は四肢形成に至らなかったのである。
また、軟骨形成や遺伝子発現パターンから、この構造は神経を遊走させた場合に生じる完全な再生芽とは異なる構造であることが強く示唆された。そこで、先年来の佐藤准教授らの研究成果である2つ再生関連因子の「FGF2」と「FGF8」というタンパク質を追加で添加したところ、軟骨形成や遺伝子発現パターンなどにおいて、神経遊走させた場合と遜色ない状況を再現することに成功し、さらに誘導した再生芽はやがて四肢構造を形成するに至ったというわけだ(画像2)。
両生類の四肢再生系では、皮膚の真皮にある細胞が再生過程で軟骨を含む結合組織の細胞種に分化できるという特徴を持つ。これは、完全に分化した組織から分化多能性を持つ未分化細胞が現れてくるということを意味している。この未分化細胞の形成は、いわば生体本来が持つ分化リセットの機構(脱分化)と考えられるという。
その点に関しても、FGF2とFGF8とGDF5では作用の違いが示された。つまり、軟骨形成に関与する細胞はGDF5を添加した細胞集団には見られず、FGF2とFGF8を添加した細胞集団にのみ現れたのである。得られた因子について、今後、より詳細な検証を加えることで、生体本来の持つ脱分化作用を明らかにすることができると考えているとした。
今回の成果は、人為的かつ人工物によって高次構造の再生を誘導したという点において大きな進展といえる。有尾両生類において「再生薬」として働き得る物質を明らかにしたことで、今後この「再生薬」がより高等な動物でどう働くのかという観点から、器官再生研究を進めることが可能だ。
また学術的観点からも、再生開始に働く具体的な要素の解明は200年以上に渡る研究の歴史上の悲願であったことから、大きなインパクトを与えられるという。今後は、同定した2つの情報伝達経路を中心に、より効率的な「再生薬」の同定、さらには生体本来が持つ「分化リプログラミング」の研究を進めることで、より高等な動物における高次構造の再生研究に貢献することが期待されるとしている。