自治医科大学は、間脳の視床下部にある神経核の1つである「室傍核」における摂食抑制ペプチド「ネスファチン」が摂食の体内時計を構成しており、その障害が肥満における摂食リズム障害の一因となることを発見したと発表した。
成果は、自治医大医学部の矢田俊彦教授、同・Udval Sedbazar研究員らの研究チームによるもの。研究の詳細な内容は、日本時間4月10日付けで米国学術雑誌「Biochemical and Biophysical Research Communications」に掲載された。
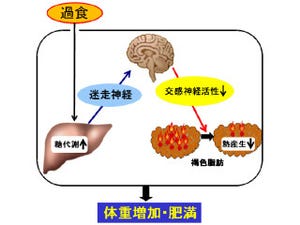
肥満と認定されるヒトは年々増加しており、全身と脳の広範な健康障害をもたらすことから、日本はもちろん、世界で大きな社会問題となっている。しかし、その発症の仕組みは十分にわかっておらず、有効で安全な治療薬がほとんどないのが現状だ。現状、肥満の主な要因の1つとされているのが、摂食亢進、つまり過食であり、また生体リズム・体内時計の障害を伴うことが多いことも注目されている。
さらに、摂食行動は動物種により特徴的なリズム(ヒトは昼間に、ラット・マウスは夜間に食べる)を持っており、その障害と肥満の関連が推察されているが、摂食を支配する体内時計の形成および障害のメカニズムはあまりわかっていない。ただし、脳の視床下部の中の室傍核が摂食を指令する中枢であることはわかっており、また自律神経やホルモン分泌における体内時計の中枢の1つとしても知られている。そして室傍核で最近発見された摂食抑制ペプチドが、ネスファチンだ。そうしたことから、研究チームはネスファチンが摂食リズムの形成に関わるかを明らかにすることを目指して研究を進めた。
正常ラットにおいては、明期早期(朝9時)に室傍核ネスファチン遺伝子の発現が上昇して反対に摂食(食餌摂取量)は低下し、そして暗期ではそれが逆転し、ネスファチン遺伝子発現が低下して摂食が上昇することが判明。室傍核ネスファチン発現と摂食行動の日内変動は、このように逆相関を示すことがわかった(画像1)。
そこで研究チームが、明期早期にネスファチン作用を阻害する抗体を脳室内に投与してみたところ、摂食が増加することが確認されたのである。さらに、室傍核選択的にネスファチン遺伝子発現を阻害したところ、ラットの摂食量が増加することが確かめられた。以上の結果より、室傍核ネスファチンは日周期を示すこと、明期のネスファチン遺伝子発現上昇は明期の摂食抑制と同調し、さらに1日摂食量の抑制にも関与することが明らかとなった次第だ。
次に肥満モデルの「Zucker fattyラット」を調べてみたところ、明期早期の室傍核ネスファチン遺伝子発現上昇が消失しており、明期の摂食量が著しく増加し1日摂食量も増加していることが判明。そこで、ネスファチン遺伝子発現上昇が障害されている明期早期にネスファチンの脳室内への投与が行われた。すると、明期の摂食亢進が著明に改善し1日摂食量増加も改善したのである。
これらの結果より、明期早期特異的な室傍核ネスファチン発現上昇が明期の摂食を抑制することにより摂食リズムの形成に関与していること、一方肥満においては明期のネスファチン発現上昇が障害されており、明期に特化した過食と摂食リズム障害の一因となっていることが解明されたのである(画像2)。
研究チームは今後、摂食リズムの形成に関与する明期早期の室傍核ネスファチン発現上昇とその肥満における障害のメカニズムを明らかにすることを目指す予定だ。まず、ラットは暗期後期にまとめ食いをするので、この食事に誘導される因子が明期早期のネスファチン発現増加をもたらす可能性を想定しているとした。
食事誘導因子の内、グルコース(ブドウ糖)とインスリンについてはすでに発表済みであることから、次は脂肪細胞によって作り出されるペプチドホルモンの「レプチン」が、室傍核ネスファチンの遺伝子発現とニューロン活動を活性化するかどうかを調べるという。さらにZucker fattyラットやヒト肥満の特徴である「レプチン抵抗性」がネスファチン発現上昇障害の原因であるかどうかも検討するとした。
また、ネスファチン発現上昇障害と不適切な時間帯の食事摂取が悪循環を形成している可能性を調べるため、Zucker fattyラットが異常な摂食亢進を示す明期に食餌を除いて食事時間帯を是正することによりネスファチン発現上昇が回復するかも調べるほか、末梢投与により室傍核ネスファチンの遺伝子発現とニューロン活動を活性化する物質を探索し、ネスファチンを標的とした肥満の時間治療を開発することを目指すとした。