物質・材料研究機構(NIMS)は10月3日、酵素の物質取り込み機能を模倣した高活性の「金ナノ粒子触媒」の開発に成功したと発表した。
成果は、NIMS 高分子材料ユニットの三木一司グループリーダーらの研究グループによるもの。研究の詳細な内容は、学術誌「Advanced Materials」に近日中に掲載される予定だ。
生体では、「ペプチド鎖」が精密に折り畳まれた3次元構造を有するタンパク質の1種である酵素が代謝経路のそれぞれの生化学反応を進行する触媒として働き、合成化学で使用されるいわゆる「金属触媒」では実現の困難な「基質特異性」や「反応特異性」などの優れた触媒機能を示す。
基質特異性とは、酵素が特定分子のみを反応対象物質として認識して反応サイトに取り込み、触媒的に分子変換を行うことをいう。生体内ではある1つの反応対象分子に着目しても、作用する酵素が違えば生成物も変わってくる。そして通常、酵素は1つの化学反応しか触媒しない性質を持ち、これを酵素の反応特異性と呼ぶ。
これら2つの特徴によって、酵素は生命維持に必要なさまざまな化学反応を行う。工業的には、反応活性が知られている酵素をデータベースとして使うのが主であり、発酵以外にも医薬品などでも幅広く利用されている。
複雑な分子構造の酵素は人工的に合成するのが難しく、現時点では微生物中の酵素を遺伝学的手法により目的に合わせて最適なものを探索する方法が主力だ。化学合成による人工酵素の開発は、今もって化学の世界では夢の1つなのである。
そうした状況の中、研究グループは今回、直径10nmの金ナノ粒子を有機分子(アルカンチオール分子)で表面修飾した構造を用いることで、金属酵素を模倣したモデル触媒構造を作製した。
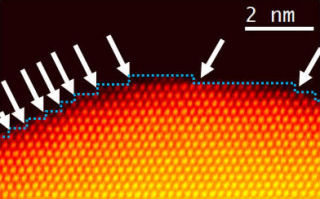
金ナノ粒子を使った人工金属酵素触媒は、1cm2の基板上に金ナノ粒子1兆個を2次元的に固定(「不均一触媒構造」)(画像1・2)。粒子を並べる手法として、アルカンチオール分子で表面修飾した金ナノ粒子同士が「自己組織化」する現象を基盤技術として利用した形だ。
有機分子の分子間力によりナノ粒子間の距離は一定になる。また、基板表面を粒子と結合できるアルカンジチオール分子で修飾しておくと、基板表面とナノ粒子との間を化学結合で固定化することが可能だ。
|
|
|
|
新型触媒の模式図。画像1(左):アルカンチオール分子で被覆された10nmの金ナノ粒子表面を平旦基板上に規則正しく配列した構造を持つ。画像2(右):走査電子顕微鏡像では、実際の金ナノ粒子のサイズが9.0nm、金ナノ粒子間の間隙が2.4nmであることがわかる |
|
新型触媒は、生体反応の触媒として生命活動を支えている金属酵素を模倣したものである。金属酵素は活性中心に金属原子を持ち、周辺を取り囲むタンパク質が非共有結合性の分子間相互作用に基づいて特定分子を活性サイトに取り込むことで、高い活性と選択性を発現したものだ。
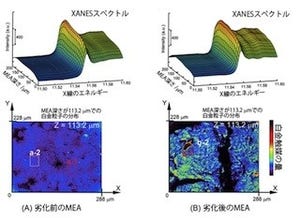
この金属酵素の構造を、アルカンチオールの自己組織化単層膜で被覆された金ナノ粒子で模倣したものが、画像3Aである。金ナノ粒子が触媒金属として働き、アルカンチオール自己組織化単層膜が金属酵素周辺部のタンパク質と類似の働きを果たすというものだ。
アルカンチオール自己組織化単層膜が内部の疎水空間に反応物質を取り込み(画像3B)、触媒である金ナノ粒子表面に反応物質を近づけることで触媒反応が効率よく進行する(画像3C、画像3D)。
具体的には、「シラン分子」とアルコール分子から「シラノール分子」を生成する「アルコホリシス反応」が新型触媒により加速されることを実証した形だ。
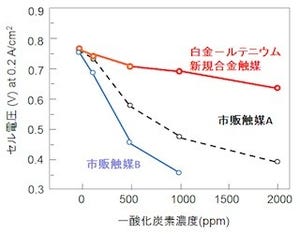
新型触媒はタンパク質と同様に、反応物質の長さやサイズを認識する機能を持つ。触媒表面のアルカンチオールとほぼ同じ長さの反応物質が最も高い活性を示す(画像4)。
一般的に酵素で見られるものと同様の触媒活性の温度依存性が観測されたことから、アルカンチオール自己組織化単層膜がタンパク質と同様のソフトな分子界面として機能していることが確認された(画像5)。
このような温度依存性は、温度上昇に伴う触媒活性の増加と共に、タンパク質の熱変性と同様に、アルカンチオールが形成するソフトな界面構造がゆらぐことで、反応物質を取り込む分子間力が弱められるために触媒加速効果がなくなり、30℃弱のところで非線形な触媒反応加速ピークが見られるのである。
アルカンチオールが形成する疎水性界面が反応物質を取り込む機能が温度上昇に伴って失われる現象は、コロイド状態における金ナノ粒子の凝集‐解離実験により別途確認された。
活性な触媒表面の金原子当たりの触媒活性は、単位時間当たりの触媒回転数(=TOF)によって評価されるが、5万5000/時間と従来の均一系触媒に比して高い数値を示した形だ。
今回の成果は、金属ナノ粒子を使って金属酵素触媒の基質取り込み機能を模倣することに成功した初めての例であり、特定の分子を選択的に取り込む機能を完全に獲得した金属酵素触媒を実現するためのブレークスルーとなる。研究グループによれば、「エナンチオ選択性」(キラル分子のような立体の鏡像異性体の分子の内、必要な方を選択的に生成する反応の性質のこと)や、より複雑な触媒機能を持つ人工触媒への応用展開が期待されるという。