国立遺伝学研究所は、植物の細胞壁合成を制御する遺伝子「IQD13」を発見し、同遺伝子が作り出すタンパク質はセルロース合成の足場となる微小管を安定化させるとともに、細胞壁合成を阻害するタンパク質の分布を制限することで、細胞壁の面積を増やす働きがあることが分かったと発表した。これにより、同遺伝子の働きを人為的に操作することでにより細胞壁の合成を制御して、セルロース生産に利用しやすい植物の作出に繋がると期待できるという。
同成果は、国立遺伝学研究所細胞空間制御研究室の小田祥久 准教授および特別共同利用研究員である杉山友希氏と、東京大学大学院理学系研究科の福田裕穂 教授、理化学研究所環境資源科学研究センター質量分析・顕微鏡解析ユニットの上級研究員である豊岡公徳氏およびテクニカルスタッフである若崎眞由美氏らによるもの。詳細は、米国科学雑誌「Current Biology」に掲載された。
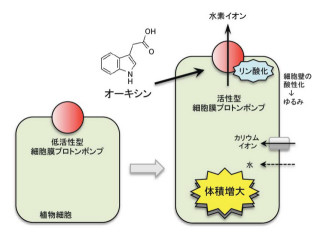
植物由来のセルロースは陸上に豊富に存在する生物資源で、紙や綿、木材などは、ほとんどがセルロースでできている。また、近年ではセルロースナノファイバーやバイオプラスチックの成分としても注目されている。セルロースは植物細胞の表面でセルロース合成酵素複合体によって合成され、セルロース微繊維という細胞壁の主成分となって細胞の外側に沈着する。このセルロース合成酵素複合体は、微小管と呼ばれる、細胞膜に密着した細長い管を足場として動きながらセルロース微繊維を合成し、細胞の表面に沈着させることが知られている。
細胞膜に密着した微小管がセルロース微繊維の沈着を適切に誘導することにより、植物細胞が成長して、植物全体が生育することができる。しかし、これまで細胞膜に密着した微小管の量や配置を制御する仕組みはよくわかっていなかった。
同研究グループは、セルロース合成酵素の足場として働く微小管の量や配置を制御する遺伝子を探すために、道管の細胞に着目した。道管は植物体内で水を通す管として働く。道管をつくる細胞は、水輸送によって生じる圧力に耐えるために、活発に細胞壁を合成する。そこで、道管の細胞で活発に働く遺伝子を調べた。その結果、IQD13という遺伝子が道管の細胞で活発に働いていることが分かった。同遺伝子が作り出す「IQD13タンパク質」を調べると、微小管に強固に結合し、微小管を壊れにくくしていることが分かった。さらに、IQD13 は細胞膜とも結合する性質を持ち、この性質により細胞膜に密着した微小管に効率よく作用していることも判明した。IQD13を過剰に作らせると、微小管が最大で3倍にまで増加した。
|
|
(左)通常の細胞の表面の内側の一部を顕微鏡下で見たもの。白い繊維が微小管。(右)IQD13の発現量を増やすと微小管が壊れにくくなり、通常よりも多くの微小管が細胞内に蓄積した。画像右下のバーは0.01mm (出所:東京大学Webサイト) |
道管の細胞では水を通す微小な孔を作るために、細胞壁合成を阻害するタンパク質が細胞膜上で働いていることが分かっている。IQD13タンパク質は細胞膜と微小管に結合しながら、このタンパク質の分布を制限し、結果的に細胞表面で細胞壁を合成する面積を増やしていることが分かった。
同研究グループは今後、IQD13遺伝子の活性を人為的に改変することにより、細胞膜に密着した微小管の量や配置を変え、細胞壁中のセルロースの量や沈着の仕方を制御することができると考え、この遺伝子改変技術を樹木や資源植物に応用することで、セルロースをより産業的に利用しやすい植物の作出に繋がる可能性を期待すると説明している。