岡山大学は、同大学異分野基礎科学研究所の墨智成准教授が"細胞内の運び屋"であるモータータンパク質「キネシン」の設計原理を、一分子計測データの数理モデリングから明らかにしたことを発表した。この研究成果は4月25日、英国の科学雑誌「Scientific Reports」に掲載された。
|
|
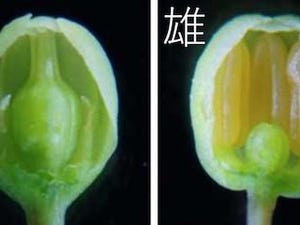
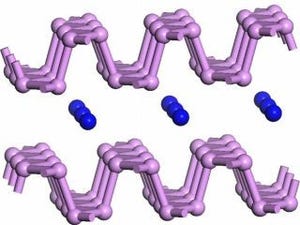
(a)細胞骨格(微小管)上を二足歩行する分子モーター「キネシン」と「ダイニン」、(b)細胞内部でキネシンは細胞体から細胞の外側へ、ダイニンはその逆方向へ細胞内物質輸送をする、(c)光ピンセット法による一分子計測実験(出所:岡山大学ニュースリリース※PDF) |
「キネシン」は、細胞骨格上を細胞の中心から外側に向かって、あたかも人間のように「二足歩行」しながら細胞内物質輸送を担うモータータンパク質のこと。これまで、この運動特性は測定されていたものの仕組みはわかっておらず、さまざまなモデルが提案されてきた。
同教授はこの問題に決着をつけるべく、キネシンの一分子計測データの数理モデリングを用いて、その「設計原理」を明らかにした。さらに、主要ワーキングサイクルは、ある特定の反応経路に固定されているわけではなく、ATPの濃度や外部負荷に応じて変化することを見出した。
また、キネシンの仲間(スーパーファミリー)以外にも、ミオシンやダイニンなどのスーパーファミリーに属するモータータンパク質が数多く発見されており、その機能や運動特性が明らかになりつつあるという。
この研究成果は、これらのモータータンパク質が、細胞内に多数存在する細胞骨格系分子モーターとしての生体機能および運動特性を発揮するために、進化の過程で獲得してきた「設計原理」の統一的理解に向けた、重要な知見であるとしている。