東京大学(東大)は6月29日、筋萎縮性側索硬化症(ALS)の発症原因に根ざした新規治療法の開発に成功したと発表した。
同成果は、国際医療福祉大学臨床医学研究センター 郭伸特任教授(東京大学大学院医学系研究科講師)、東京大学大学院医学系研究科 脳神経医学専攻 神経病理学分野 赤松恵特任研究員、山下雄也特任研究員らの研究グループによるもので、6月28日付の英国科学誌「Scientific Reports」に掲載された。
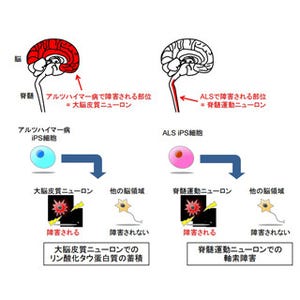
ALSは、運動ニューロンの変性によって進行性の筋力低下や筋萎縮を起こし、健康人を数年内に呼吸筋麻痺により死に至らしめる神経難病で、この経過を遅らせる有効な治療法はいまだ見つかっていない。
同研究グループはこれまでに、ADAR2という酵素の発現低下が、過剰な細胞内カルシウム流入を引き起こし、ALS患者の大多数を占める孤発性ALSの運動ニューロン死に関与していることを突き止めていた。
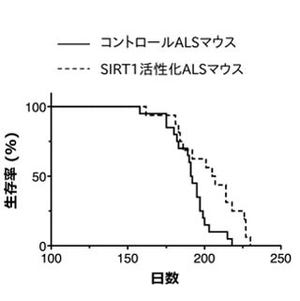
今回、同研究グループは、孤発性ALSの病態を示すコンディショナルADAR2ノックアウトマウス(AR2マウス)を開発。過剰な細胞内カルシウム流入を抑える作用が期待される既存の抗てんかん薬「ペランパネル」を同マウスに90日間連続で経口投与したところ、運動機能低下の進行とその原因となる運動ニューロンの変性脱落が食い止められることがわかった。さらに、運動ニューロンで引き起こされているALSに特異的なTDP-43タンパクの細胞内局在の異常が回復・正常化することも明らかになった。また、この効果は、症状が進行した時期のマウスにおいても確認されている。
ペランパネルはすでに国内外で承認されているてんかん治療薬であり、今回、ヒトに換算した場合にてんかん治療に要する用量以下でマウスに有効性が確認出来たことから、同研究グループは臨床応用へのハードルが低いと考えており、ALSの特異的治療法になることが期待されるとしている。