岡山大学は、光合成による水分解反応を触媒する光化学系II複合体の構造を1.95Åの分解能で突き止めることに成功したと発表した。
同成果は、岡山大学大学院自然科学研究科の沈建仁 教授(同大光合成研究センター長)、菅倫寛 助教、秋田総理 助教、理化学研究所 放射光科学総合研究センター利用システム開発研究部門ビームライン基盤研究部の山本雅貴 部長、同生命系放射光利用システム開発ユニットの吾郷日出夫 専任研究員らによるもの。詳細は11月26日(英国時間)に、英国の科学雑誌「Nature」に掲載された。
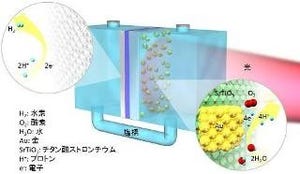
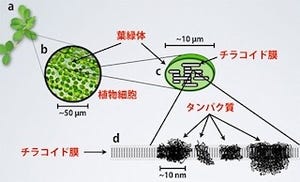
藻類や植物が行う光合成の酸素発生反応は、葉緑体にある「光化学系II複合体」と呼ばれる19個のタンパク質から構成されるタンパク質複合体によって行われている。
これまで研究グループは日本の温泉由来のラン藻の一種から取り出した光化学系II複合体の結晶を作成し、その構造をSPring-8の放射光X線を用いて1.9Åの分解能で解析を行い、その成果を報告していたが、X線結晶構造解析で使用するX線回折写真の撮影に必要な数秒間のX線照射の間に、水分解反応を担う触媒中心の一部がX線による放射線損傷を受け、本来の構造とわずかに異なっている可能性があったという。
そこで今回の研究では、X線による放射線損傷の影響のない光化学系IIの本来の構造の解析を目指し、X線自由電子レーザー(XFEL)施設「SACLA」を用いて実験が行われた。XFELは1パルスでX線回折写真を撮影でき、かつ、1パルスの継続時間が10フェムト秒と短いため、X線による放射線損傷で分子の構造変化が起こる前に、X線回折写真を撮影することが可能という特徴がある。
具体的にはSACLAで開発した「フェムト秒X線結晶構造解析法」と世界最高品質の光化学系IIの結晶を作成する技術を組み合わせることで、光化学系II複合体の放射線損傷を受けていない本来の構造を、1.95Å分解能で解析することに成功。その結果、これまでSPring-8の放射光を用いて得られた構造よりも原子間の距離が0.1~0.3Å程度短くなっていることが判明したという。
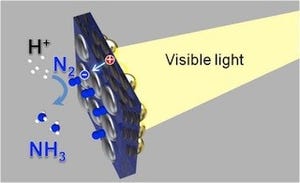
光化学系IIの触媒中心である「Mn4CaO5クラスター」は周りのアミノ酸が協調的に構造変化することで、周期的な5つの中間状態を経て高効率の水分解反応が行われるが、その動的メカニズムの詳細は不明となっている。研究グループでは、今回の成果について、光化学系IIの反応周期の第一状態について反応性を維持したままの本来のMn4CaO5クラスターと周辺の構造を明らかにしたものであり、太陽の可視光エネルギーを利用した水分解反応を人工的に実現するための触媒の構造基盤を提供することにつながるとしており、この反応を模倣した「人工光合成」が実現すれば、光エネルギーを高効率で電気エネルギーや化学エネルギーに変換することにつながり、エネルギー問題や環境問題、食糧問題など解決につながることが期待されるとコメントしている。