筑波大学は1月20日、東京大学、米カリフォルニア大学の協力を得て、遺伝子発現を調節する働きを持つタンパク質「MafB」が、白血球の1種である「マクロファージ」の「アポトーシス(プログラム細胞死)」を阻害することで、動脈硬化の病態を悪化させることを発見したと発表した。
成果は、筑波大医学医療系、生命領域学際研究センターおよび国際統合睡眠医科学研究機構の濱田理人 助教、同・中村恵弥博士、同・高橋智 教授、同大学 内分泌代謝・糖尿病内科の島野仁 教授、東大大学院医学系研究科 疾患生命工学センター 分子病態医科学部門の宮崎徹教授、カリフォルニア大のピーター・トントノズ教授らの国際共同研究チームによるもの。研究の詳細な内容は、日本時間1月20日付けで英オンライン科学誌「Nature Communications」に掲載された。
免疫細胞の1つであるマクロファージは、外界から侵入した細菌などの有害なものに対して防御的に働いたり、体内の老廃物などのゴミを取り除いたりして体をきれいな状態に保っている。しかし、動脈硬化症においてはマクロファージのこの機能がむしろ病態に悪く働いてしまう。
動脈硬化では、高血圧や糖尿病などによって血管に負担がかかると、血中の脂質であるLDLコレステロールが血管内皮下に入り込み、酸化される。この酸化されたLDLコレステロール(酸化LDL)は悪玉コレステロールとも呼ばれるように、周りの細胞に対して毒性を持つことから、これを取り除くためにマクロファージが集まってくる。
過剰に酸化LDLが存在すると、それを取り込んだマクロファージ細胞内には酸化LDLの分解産物による油滴ができ、泡沫化してしまう。これを「泡沫細胞」といい、この泡沫細胞が蓄積することで血管内膜はどんどん厚くなり、動脈硬化が進行してしまうというメカニズムだ(画像1)。近年の解析により、動脈硬化初期病変の進行には、マクロファージのアポトーシスが関与していることがわかってきた。
MafBは転写因子だ。転写因子とは、DNAの特定の部位に結合することで、標的遺伝子のスイッチをオンにしたりオフにしたりする機能を持つ。MafBがマクロファージで発現していることは知られており、1990年代から多くの研究チームが精力的にMafBの機能解析を行ってきた。しかし、マクロファージが血管内皮下に留まる詳しい仕組みも、マクロファージにおけるMafBの具体的な機能もこれまでのところは明らかになっていない。そこで今回の研究チームは疾患に関連したマクロファージに注目し、MafBの機能の解明を行うことにしたのである。
今回の研究に先立ち、研究チームは、MafBが生体内でどのような働きをするのかを調べるために、MafBを産生できない「MafB欠損マウス」を2006年に作製。今回、さらに移植実験により血液細胞のみMafBを欠損した動脈硬化モデルマウスを作製し、動脈硬化の病態変化が検討された。
ちなみに移植実験の内容は、X線を照射することにより動脈硬化モデルマウスの造血系細胞を破壊し、そこにMafB欠損マウス由来の造血幹細胞を多く含む胎児肝臓細胞を静脈注射により移植したというもの。移植後2カ月以上経つと、ほぼ完全にMafB欠損マウス由来の血液か置き換わる。
実験の結果、血液細胞MafB欠損マウスでは動脈硬化病変部の面積(脂肪の蓄積)が減少することが明らかとなった(画像2・3)。また、このマウスの病変部ではアポトーシスが増加しており、アポトーシス抑制タンパク質「AIM」の発現が著しく減少していた(画像4)。
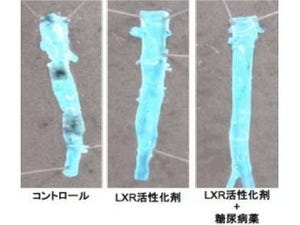
さらに、MafBがどのようなシグナルを受けてAIMを制御しているのかが検討され、その結果、酸化コレステロールによって活性化された核内受容体型転写因子「LXR」がMafBを制御していることが、LXR欠損マウスの解析により明らかとなったのである(画像5)。
なお核内受容体型転写因子とは、転写因子の1種だ。ただし、それ自体がある特定のホルモンや分子と結合することにより活性化されて、遺伝子の発現を制御する仕組みを持つ。例えば、LXRは酸化LDLの分解産物「オキシステロール」と結合することにより、標的遺伝子の発現を調節することが明らかとなっている。
今回の結果から、酸化LDLからのシグナルにより活性化したLXRがMafBのタンパク質発現を促し、さらにMafBがAIM遺伝子の発現を制御することによって、泡沫細胞のアポトーシスを起こりにくくさせ、動脈硬化を進行させることが明らかとなった(画像6)。
今回の成果などにより、MafBがAIM遺伝子の発現を調節する機構は今のところ動脈硬化病変部でのみ観察されていることから、このメカニズムをターゲットにした新しい動脈硬化治療法の開発が期待されるとしている。