生理学研究所(NIPS)は10月25日、米ベイラー医科大学との共同研究により、氷に封じられた細胞やウイルスを生状態で観察することが可能な、電子顕微鏡の1技術「急速凍結法」の"像のコントラストが弱く微小形態の特定が困難"という課題を解決する「位相差クライオ電子顕微鏡法」を用いて、シアノバクテリアに感染したウイルスの立体構造形成の解明に応用したことを発表した。
成果は、NIPSの特別研究の永山國昭 特任教授、米ラー医科大のWah Chiu教授らの国際共同研究チームによるもの。研究の詳細な内容は、10月31日付けで英科学誌「Nature」に掲載された。
無染色で透明な生きた細胞の微細観察を最初に可能としたのは、光学顕微鏡の「位相差法」で、オランダのFritz Zernike氏により発明され、同氏はその功績で1953年のノーベル物理学賞を受賞した。それと同じ方法を電子顕微鏡に応用する試みも行われるようになり、それは光学顕微鏡ほど早い時期には達成されず、50年以上かかり、科学技術振興機構の支援を受けて2005年に永山特任教授らの手によって開発されたのである。この段階では「透過電子位相顕微鏡」と呼ばれ、後に「クライオ(低温)」機能を付加したのが今回利用された位相差クライオ電子顕微鏡というわけだ。
急速凍結法の開発により、ホルマリン漬けにしたり、重金属で染色したりする破壊的試料作成を行わずに済むようになったが、冒頭で述べたように、像のコントラストが弱く微小形態の特定が困難という課題があった。それを解決したのが位相差クライオ電子顕微鏡だが、その開発のカギとなったのが、位相差法の心臓部である薄い炭素膜でできた位相板の帯電防止法の確立だった。
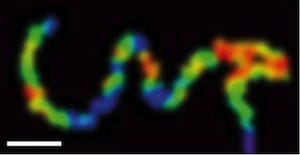
今回の位相電子顕微鏡法を用いて、共同研究者のWah Chiu教授率いるベイラー医科大のグループにより、地球上において炭酸ガス固定の主役であるシアノバクテリアに感染したウイルスの立体構造が形成される様子が解明された(画像1)。感染初期にまずウイルスの外殻ができ、次にDNAゲノムがその中に封入され、最後に角や尾ができる形作りの過程(画像2)が明らかにされ、ウイルス感染の生活史モデルが提出された(画像3)。
今回の成果により、位相電子顕微鏡法は、医学生物学研究の最先端を切り拓く有力な方法であることが実証された形だ。またシアノバクテリアのウイルス感染生活史の解明を通じ、CO2問題の解決につながる期待および位相差電子顕微鏡法によりヒトウイルス感染の詳細が解明され、予防や治療につながる期待があるとしている。
そして位相電子顕微鏡法を開発した永山特任教授は「今回の研究で、10年来地道に続けてきた位相差電子顕微鏡の開発研究が医学、生物学分野で正しく評価されることを期待しています」とコメントした。