慶應義塾大学(慶応大)は8月29日、慢性の「移植片対宿主病(GVHD)」のマウスモデルを用いたドライアイの病態解明の研究で、重症ドライアイにおける「免疫応答」の発症機構に、炎症細胞の1つである「マクロファージ」の老化が関与していることを見出したと発表した。
成果は、慶応大医学部 眼科学教室の小川葉子特任准教授、同・榛村重人准教授、元・同大学病院医師の河合正孝医師(非常勤)、同・眼科学教室主任の坪田一男教授、同・医学部 先端医科学研究所 細胞情報研究部門主任の河上裕教授らの研究チームによるもの。研究の詳細な内容は、欧州西部時間8月29日付けで英オンライン総合学術誌「Scientific Reports」に掲載された。
眼表面には、角膜(黒目)や結膜(白目)、涙腺(涙の水成分を作る器官)、副涙腺、マイボーム腺(涙の油成分を作る器官)などが存在する。涙はこれらの眼表面組織を保護し、物が鮮明に見えるための光学的透光体としての役割や眼の表面の健常性を保つ役割を担っている。眼表面組織は一体化した粘膜上皮に覆われ、これらのどの部位が障害されても眼表面の恒常性が維持されなくなってしまう。そして涙の働きが不安定になり、ドライアイが生じてしまうのである。
血液悪性疾患などの根治療法としての造血幹細胞移植の後に、約半数の患者が発症するとされる晩期合併症の1つ慢性GVHD(移植後1~2週間後に発症する急性GVHDとは区別される)や、涙腺や唾液腺などにリンパ球浸潤が生じ、涙液や唾液の分泌を障害する自己免疫疾患の1種である「シェーグレン症候群」など、免疫応答が関与するドライアイはこれらのさまざまな要素が影響し合った結果として炎症が引き起こされる。なお免疫応答とは、免疫反応の役割をする細胞が体の外因性または内因性の異物を自分の体の一部ではない抗原として認識し、特異的に行われる反応のことだ。
慢性GVHDやシェーグレン症候群などが、白血球をはじめとする炎症性細胞が炎症の起きている組織に侵入する「炎症性細胞浸潤」により角膜、結膜や涙腺の機能が悪くなって発症することはわかっていたが、その発症や病気の進展のメカニズムにはまだ不明な点が数多く残されていた。
慢性GVHDの免疫応答による重症ドライアイ症例に、まつ毛、眉毛および毛髪の白髪化がドライアイと共に生じる場合が認められ、結膜腫瘤の発生率が高くなると報告されている。そこで今回の研究では、このタイプのドライアイに何らかの老化現象が関与するという仮説を着想し、慢性GVHDによる免疫原性ドライアイのマウスモデルの涙腺における免疫応答と老化との関連が調べられた。
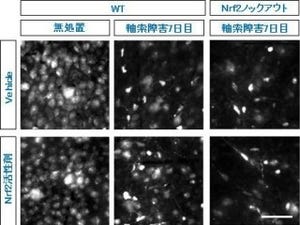
研究チームは、ヒトの免疫応答を再現する慢性GVHDマウスモデルを用いて特に涙腺に焦点を当てて研究を実施。まず若年マウス、老齢マウス、慢性GVHDマウスモデル、GVHDコントロールマウスの涙腺が調べられ、その結果、慢性GVHDマウスモデルにおいて、老齢マウスと同じように線維化や、炎症性細胞浸潤を来していることが判明した。
さらに電子顕微鏡による解析で詳細を検討すると、老齢マウスと同じように慢性GVHDマウスモデルにおいて細胞内小器官「ミトコンドリア」の形態異常が認められ、脂質が含まれる高度に酸化された変成タンパク質「リポフスチン」が蓄積していることがわかったのである。
さらに慢性GVHDマウスモデルでは、涙を産生する涙腺に浸潤する炎症細胞に老化マーカーの「p16」や酸化ストレスマーカーの「8-OHdG」(DNA損傷マーカー)、「4-HNE」(脂質酸化マーカー)、「HEL」(脂質酸化マーカー)が発現していることも見出された。
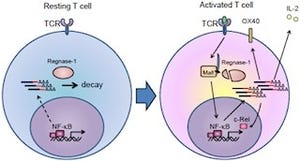
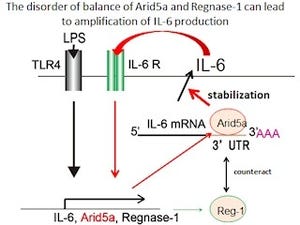
涙腺の微小環境下で、特に酸化ストレスマーカーを発現する免疫担当細胞はマクロファージ(白血球の1種の生体内を遊走する貪食細胞)であり、同じく免疫細胞の1種である「T細胞」と接着して何らかの情報交換をしていることも確かめられている(画像1~4)。
|
|
|
|
慢性GVHDマウスモデル涙腺組織での免疫担当細胞における酸化ストレスマーカーの発現。画像3(左):涙腺導管周囲に浸潤するT細胞(赤、矢印)は多くの8-OHdG(白△の部分、緑色の細胞)を発現する浸潤細胞に接着していた。画像4(右):8-OHdGを発現する炎症性浸潤細胞はマクロファージ(CD68、赤)であることがわかった。(白△の部分、黄色の細胞) |
|
老齢マウス、慢性GVHDマウスモデルの涙腺では若年マウスとコントロールマウスの涙腺に比べて、顕著に酸化ストレスタンパク質(脂質の酸化マーカー)のHELの発現が上昇していることも確認された。画像5は、それを表した、涙腺におけるHELの発現に関するグラフだ。老齢マウスと慢性GVHDマウスモデルの涙腺には、HELのタンパクの発現がコントロールマウスと若年マウスに比べて亢進していることが判明。免疫ブロット(ウェスタンブロット)という方法でタンパクの発現が確認された。
これらの事実から、涙腺に浸潤するマクロファージの老化が、ドライアイを来す涙腺の病態の発症から慢性炎症へと進展していく過程で主要な役割を果たしている可能性が見出されたというあけだ(画像6)。
免疫応答の関与する慢性GVHDマウスモデルを検討することにより、ドライアイの発症時期や経時的な変化、進展を正確にとらえられる。そのため、今後、免疫応答によるドライアイと老化の関係だけでなく、老化のメカニズムを解明する手がかりとなると考えられ、がんや動脈硬化等生命予後に関わる疾患の病態解明にも役立つ可能性があるという。
またマクロファージの老化は動脈硬化ばかりでなく、眼の加齢疾患の代表ともいえる「加齢黄斑変性」においても重要な要因であることが近年わかってきており、今後、免疫応答の異常と老化メカニズムの関連性を解明することに貢献することが期待されるとしている。