京都大学は12月7日、ヒト人工多能性幹(iPS)細胞中の全タンパク質(プロテオーム)に対し、独自の計測システムを用いた発現解析を行い、約1万種のタンパク質の発現量プロファイルを取得することに成功したと発表した。
成果は、京大 薬学研究科の石濱泰教授、iPS細胞研究所(CiRA)の中川誠人講師、同・山中伸弥所長(教授)らの共同研究グループによるもの。研究の詳細な内容は、12月4日付けで「Journal of Proteome Research」に掲載された。
タンパク質は細胞の機能制御の主役であり、機能解析をする上でその全体像(プロテオーム)をとらえることが必須だ。しかし、タンパク質の設計図であるゲノムや遺伝子に比べるとその計測は困難であり、ヒトゲノムやヒト遺伝子が明らかになった現在でも、ヒトタンパク質の全貌はわかっていない。
このヒトプロテオームのすべてを明らかにすることを目的とした「ヒトプロテオームプロジェクト」が、現在ヒトプロテオーム機構による国際プロジェクトとして進行している。石濱教授らはこのヒトプロテオームプロジェクトの日本チームの一員であり、大規模プロテオーム解析のための独自の計測システムの開発に取り組んでいるところだ。
今回の研究では、自家製のメートル長キャピラリーカラムを用いる独自の「ナノ液体クロマトグラフィー-タンデム質量分析(nanoLC-MS/MS)」システムである「ワンショットプロテオミクスシステム」を用いて解析が行われた。
iPS細胞は山中教授らによる発見以来、多くの研究者らによってその多能性獲得や多能性維持機能の研究が行われているが、未だにその詳細なメカニズムは明らかになっていない。
研究チームは、iPS細胞機能解析に必須の基盤情報であるタンパク質の発現量情報の取得を目的とし、iPS細胞とその誘導前に当たるヒト線維芽細胞中のプロテオームプロファイルとの発現比較を行い、iPS細胞の発現プロテオームプロファイルを明らかにした。さらに、情報学的検討を加え、その特徴付けが行われた形だ。
具体的にはCiRAにて樹立されたヒトiPS細胞5株および対照試料としてヒト線維芽細胞3株を用意し、研究グループが開発した独自のプロトコール「相間移動可溶化法」を用いてタンパク質を高収率で抽出。さらに消化酵素トリプシンで処理して、ペプチド試料溶液を調製。nanoLC用カラムとして、内径0.1mm、長さ2mのガラス製毛細管内部にシリカモノリスと呼ばれる多孔性連続構造体を重合反応により調製した。
このカラムをnanoLC-MS/MS装置に搭載したワンショットプロテオミクスシステム(画像1)を用い、ペプチド試料を前分画なしで1試料あたり10時間かけ、ゆっくりとnanoLCからMS/MS装置に溶出させて直接計測を行ったのである。そして得られたデータを情報学的手法により解析され、それぞれの試料溶液に含まれているタンパク質が同定・定量された。
その結果、ヒトiPS細胞5株および線維芽細胞3株より合計9510種のタンパク質を同定することに成功(画像2)。これは、現在報告されているiPSプロテオーム研究としては世界最大のもので、従来のものよりも50分の1以下の試料量で3倍の高速測定が可能だった。
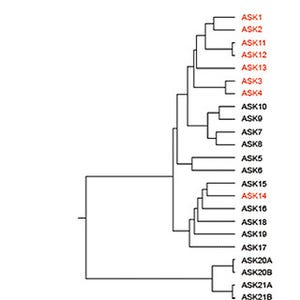
次に、それぞれの細胞株におけるタンパク質発現プロファイルについて、お互いにどのくらい似ているかを調べるため、クラスター解析も実施(画像3)。その結果、iPS細胞同士、線維芽細胞同士はとてもよく似ており、iPS細胞と線維芽細胞では約40%のタンパク質がどちらかに選択的に発現していることがわかったのである。
そこで、どのようなタンパク質が選択的な発現パターンを示すのかが調べられ、転写制御に関わるタンパク質がiPS細胞により多く発現していることが判明した(画像4・A)。そしてこのグループには人工多能性を誘引する山中4因子やすでに多能性マーカーとして知られているタンパク質群も含まれていることが確認されたのである。
今回の研究では国際ヒトプロテオームプロジェクトの一環として、タンパク質として今まで存在が確認されていなかった6244種のタンパク質についても注目。解析が進められたところ、1091種のタンパク質の発現を確認することに成功した。その内、転写制御機能を持ち、iPS細胞選択的に発現している5種類のタンパク質が同定されたのである。
そのほか遺伝子解析では、解析不可能なタンパク質の翻訳後修飾に関わる情報に注目し、糖(グリコシル化)(画像4・B)、メチル化(画像4・C)およびリン酸化(画像4・D)についても調べられた。すると、糖修飾については線維芽細胞で、メチル化についてはiPS細胞でより亢進していることがわかったのである。
なお、リン酸化酵素キナーゼ全体では明確な分布の偏りは見られなかったが、個々のキナーゼについてはどちらかの細胞に偏ったものも観測された。
今回の研究では、世界最大のヒトiPSプロテオーム情報を取得することに成功し、そのプロファイルが明らかにされた。これらの成果はヒトiPSプロテオーム研究の第1歩となるもので、研究チームではさらに翻訳後修飾プロテオーム解析などが進められていく予定だ。これらの情報はヒトiPS細胞のさまざまな機能解析を行う上での基盤情報となるものであり、iPS細胞研究全体が加速することが期待されると、研究グループはコメントしている。