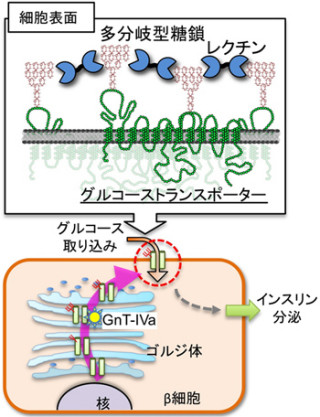
産業技術総合研究所(産総研)は、ラットを用いた動物実験で、成体の神経幹細胞を膵臓に移植する糖尿病の再生医療(画像1)に有効な方法を開発し、その治療効果を確認したと発表した。産総研浅島誠フェローや、産総研幹細胞工学研究センター幹細胞制御研究チーム桑原知子主任研究員らと、米ソーク研究所のFred H. Gage教授との共同研究のによるもので、成果は欧州の学術誌「EMBO molecular medicine」に掲載される予定だ。
近年、日本における糖尿病患者の数は激増しており、予備軍などを含めると1000~2000万人にも及ぶとされる。糖尿病は、発症後に多くの患者が網膜症や腎症などの合併症に至る重症化を引き起こす。そのため、糖尿病に対する根本的な治療法の確立が、重要課題の1つとなっている。
I型糖尿病の治療法としては、他人の膵臓からの膵島(ランゲルハンス島)移植は効果があるが、誰の膵臓でもいいというわけではない。消化酵素で満たされている膵臓特有の性質から、適合性のある提供可能者を見つけておかないと移植可能な膵臓が入手できない。そのため、ほかの臓器と同様に膵島移植医療のドナー不足の問題は非常に深刻である。
また幹細胞移植という膵島移植に代わる移植治療法もあるが、こちらは移植に用いる幹細胞を、いかに効率よく安全に用意できるかが課題だ。移植後の患者の長期にわたる生活の安定のために、将来がん化などを引き起こしかねない遺伝子導入などの操作を行わず、移植先の臓器に順応する性質を持つ、より安全な幹細胞が求められているのである。
成体の脳内には、「神経新生」を起こしている神経幹細胞が存在する。そして、成体の神経幹細胞についての基礎的な研究の過程で、インスリンを産生するために必要な遺伝子が、成体の膵臓と脳の神経系で共通して発現していることも見出された。さらに、近年わかってきたのが、神経幹細胞が成体期の「鼻嗅球」(びきゅうきゅう)にも存在すること。嗅球とは嗅覚の情報処理に関わる、脊椎動物に備わる神経の組織だ(ヒトの場合は、鼻腔の奥にある「嗅細胞」が鼻嗅球)。
自家細胞を採取して移植用の細胞源として用いる再生医療への応用を考えると、困難な手術を伴うよりも内視鏡などを用いて採取できる方が望ましく、鼻嗅球に存在していることが確認されたのは幸運といえる。そのため、鼻嗅球からの神経幹細胞を採取・樹立する方法の研究が始められた。
そこでまず、脳の海馬と鼻嗅球の成体神経幹細胞を比較することに。ラットの脳の海馬と鼻嗅球の両方から樹立・培養。インスリン産生に必要な遺伝子や、分化に重要な遺伝子などがどのように発現されるかについて、マイクロアレイ法などを用いて遺伝子の発現比較解析が行われた。その結果、海馬由来、鼻嗅球由来どちらの神経幹細胞でも、神経細胞に分化する過程でインスリンを産生する遺伝子が発現することが判明したのである。
次に、糖尿病のラットの脳海馬と鼻嗅球から、それぞれ神経幹細胞を樹立して、実際に移植の効果を調査した。まず、インスリンの産生能力を促進させる薬剤を添加した細胞培養液中で2週間ほど、神経幹細胞を培養。その後に糖尿病ラットの膵臓に移植し、糖尿病の病態を表す血糖値を定期的に測定した。
すると、海馬由来と鼻嗅球由来のどちらの神経幹細胞を移植した系でも、糖尿病ラットの血糖値が徐々に減少し、糖尿病の病態が改善された。なお、神経幹細胞を移植しなかった糖尿病ラット群は8週間後には(画像2の*)、病態が顕著に悪化して死亡した。さらに病態が改善した糖尿病ラットから移植した神経幹細胞を除去したところ(画像2の点線矢印)、血糖値が再び上昇した。
さらに成体神経幹細胞の移植後15週間経過した糖尿病ラットの膵臓で、インスリンがどの細胞から産生されているかを抗体染色で調査。移植した成体神経幹細胞と糖尿病ラット由来の細胞を識別するために、移植細胞は緑色蛍光タンパク質(GPF)をマーカーとして発現するようにした。糖尿病ラットの膵臓の膵島では、インスリンはほとんど産生されていないが、対照的に移植した神経幹細胞(画像3、緑の細胞)からは、効率よくインスリンが産生されていることが確認された。これらの結果は、糖尿病ラットの納会場や鼻嗅球から樹立した神経幹細胞が、移植された膵臓内でインスリンを産生することにより、糖尿病の病態が改善されたことを示したといえる。
|
|
|
画像3。移植された成体神経幹細胞がインスリンを産生している様子。上は成体神経幹細胞が移植されていない膵臓で、糖尿病ラットの膵臓では、インスリンがほとんど産生されていないのがわかる。一方、下は成体神経幹細胞が移植された糖尿病ラットの膵臓。緑色のものが移植された成体神経幹細胞で、赤が産生されたインスリンを示す |
今回開発した技術は自家細胞の移植なので、ドナー問題はなく、免疫抑制剤による副作用の心配もないため、より自然な再生医療につながると考えられている。インスリンを産生する細胞が継続的に成体神経幹細胞から補充され、治療効果が長く持続することが利点だ。また、遺伝子導入過程を一切含まないのでがん化などのリスクが低く、安全性も高い。重度の合併症を引き起こす前段階の予備治療としても利用でき、可能となる治療対象は幅広いと考えられているとした。
なお、今後の予定としては、成体の神経幹細胞でインスリンが産生されるメカニズムの解析から得られた知見をもとに、神経細胞そのものに与える影響や、より効果的なインスリン産生能力の活性化薬剤の探索に向けた研究を行うとしている。